Odniesienia
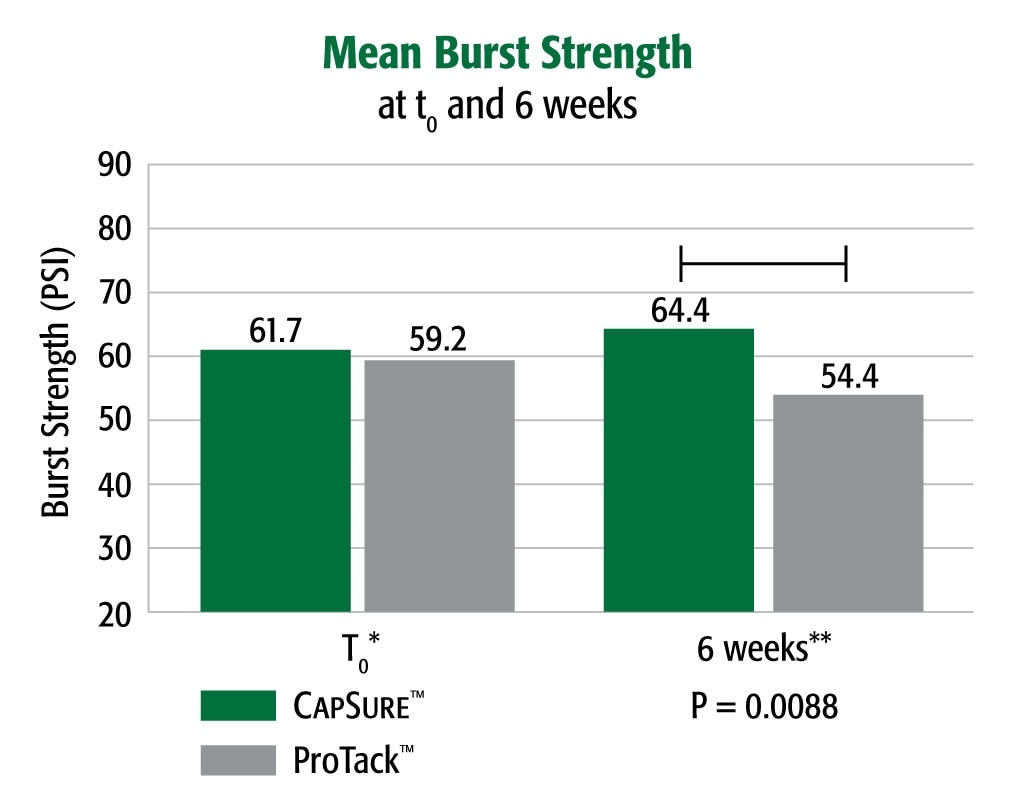
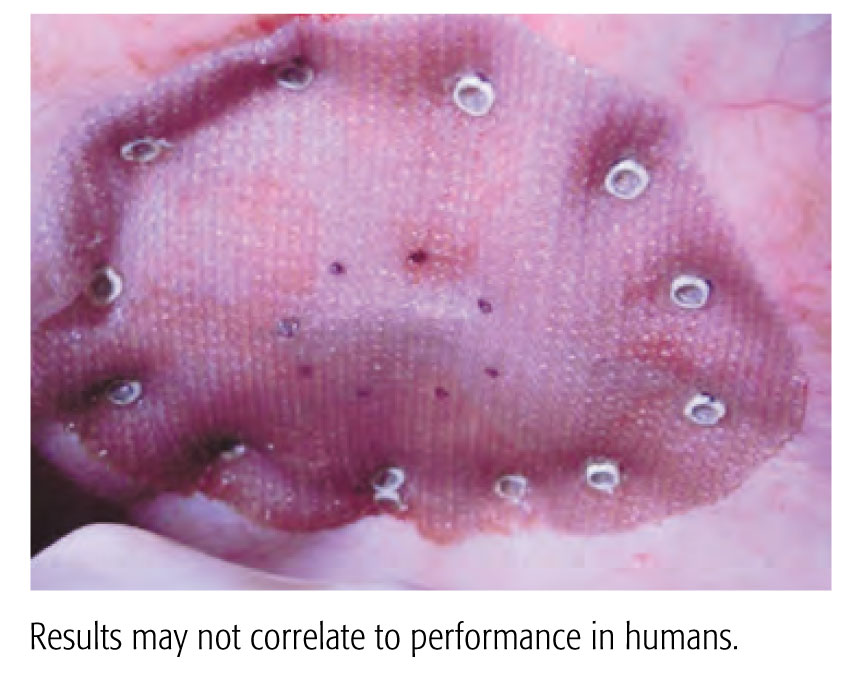
Dane uzyskane w badaniach laboratoryjnych. Wyniki mogą nie przekładać się na skuteczność u ludzi
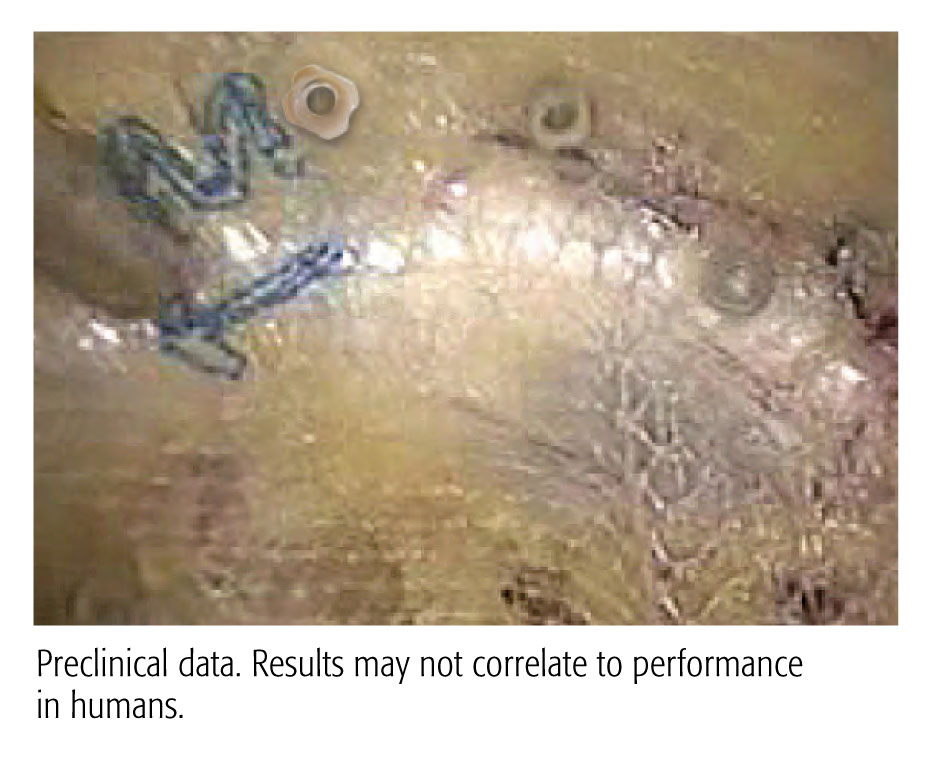
Dane przedkliniczne. Wyniki mogą nie przekładać się na skuteczność u ludzi
Zastrzeżenia
Nie wszystkie produkty, usługi, oświadczenia lub funkcje produktów mogą być dostępne lub ważne w regionie użytkownika. Należy skontaktować się z lokalnym przedstawicielem firmy BD.
Wszelkie wskazania, przeciwwskazania, zagrożenia, ostrzeżenia, środki ostrożności znajdują się na etykietach i w instrukcjach użycia.
Wskazania
System do trwałego mocowania CapSure™ jest przeznaczony do przybliżania tkanek miękkich i mocowania do nich siatki chirurgicznej podczas laparoskopowych zabiegów chirurgicznych w ramach leczenia brzusznej i pachwinowej.
Przeciwwskazania
Ten produkt nie jest przeznaczone do użycia w inny sposób niż wskazany.
Nie używać tego produktu w sytuacji, gdy nie można wzrokowo potwierdzić uzyskania hemostazy po zastosowaniu.
Przeciwwskazania związane z laparoskopowymi procedurami chirurgicznymi związane z mocowaniem siatki, w tym między innymi: mocowanie struktur naczyniowych lub nerwowych oraz w tkance niedokrwionej lub martwiczej.
Należy dokładnie skontrolować obszar w pobliżu mocowania tkanki, aby uniknąć niezamierzonej penetracji struktur leżących poniżej, takich jak kość, nerwy, naczynia i narządy wewnętrzne. Stosowanie systemu stałego mocowania CapSure™ w bliskim sąsiedztwie takich struktur jest przeciwwskazane. Dla porównania, długość elementu mocującego poniżej nasady wynosi 3,2 mm, a nasada elementu mocującego to kolejny 1 mm (łącznie 4,2 mm).
Produkt nie powinien być stosowany w tkankach, które są bezpośrednio powiązane anatomicznie z głównymi strukturami naczyniowymi lub nerwowymi. Podczas leczenia przepukliny przeponowej, obejmuje to również umieszczanie elementów mocujących w przeponie w pobliżu osierdzia, aorty lub żyły głównej dolnej.
Ostrzeżenia
System stałego mocowania CapSure™ jest przeznaczony tylko do jednorazowego użytku — NIE STERYLIZOWAĆ PONOWNIE. Ponowne użycie, przetwarzanie, wyjaławianie lub przepakowanie może naruszyć integralność strukturalną i/lub zasadnicze właściwości materiału oraz konstrukcji, które są kluczowe dla ogólnego działania siatki i mogą prowadzić do jej uszkodzenia, co może skutkować obrażeniami pacjenta. Ponowne użycie, przygotowanie do ponownego użycia, ponowna sterylizacja lub przepakowanie może również stworzyć ryzyko zanieczyszczenia siatki i/lub spowodować zakażenie pacjenta lub zakażenie krzyżowe, w tym między innymi przeniesienie chorób zakaźnych z jednego pacjenta na drugiego. Zanieczyszczenie produktu może prowadzić do obrażeń, choroby lub śmierci pacjenta lub użytkownika końcowego.
Nie używać po upływie daty ważności podanej na opakowaniu.
Dostarczany produkt jest jałowy. Przed użyciem należy sprawdzić opakowanie w celu upewnienia się, że jest nieotwarte i nieuszkodzone.
Przed wspólnym zastosowaniem wyrobów od różnych producentów w ramach jednego zabiegu, należy sprawdzić ich kompatybilność mechaniczną i elektryczną.
Przed użyciem protezy powinny być ocenione pod kątem kompatybilności.
Przed zastosowaniem elementów mocujących systemu CapSure™ do zamykania rany, użytkownicy powinni być zaznajomieni z procedurami i technikami chirurgicznymi z wykorzystaniem materiałów do stałego mocowania, ponieważ ryzyko rozejścia się rany może się różnić w zależności od miejsca zastosowania i użytego materiału.
Podobnie jak w przypadku każdego materiału implantologicznego, produkt może nasilać zakażenie bakteryjne ran. Należy przestrzegać przyjętej praktyki chirurgicznej w odniesieniu do drenażu i zamykania zakażonych lub zanieczyszczonych ran. Po użyciu, system stałego mocowania CapSure™ może stanowić zagrożenie biologiczne. Używać i utylizować zgodnie z wszystkimi lokalnymi i federalnymi przepisami dotyczącymi odpadów medycznych.
Środki ostrożności
Przed zastosowaniem systemu stałego mocowania CapSure™ należy przeczytać wszystkie instrukcje.
Zabiegi chirurgiczne powinny wykonywać jedynie osoby posiadające odpowiednie przeszkolenie medyczne i znające techniki chirurgiczne. Przed wykonaniem jakiegokolwiek zabiegu chirurgicznego należy zapoznać się z literaturą medyczną w celu uzyskania informacji na temat techniki, powikłań i zagrożeń.
System stałego mocowania CapSure™ może być stosowany z większością trokarów 5 mm. Należy zapewnić zgodność poprzez włożenie produktu w trokar przed wprowadzeniem do ciała pacjenta. System trwałego mocowania CapSure™ powinien wchodzić i wychodzić z trokara z łatwością, bez użycia nadmiernej siły. Użycie zbyt dużej siły może doprowadzić do uszkodzenia narzędzia.
Na obszar docelowy należy zastosować odpowiednio duży nacisk. Nie należy umieszczać dłoni lub palców bezpośrednio nad obszarem, w którym wprowadzany jest element mocujący, aby zapobiec obrażeniom.
Należy zachować ostrożność podczas zakładania elementu mocującego CapSure™ nad lub w pobliżu kości, naczyń krwionośnych, nerwów lub narządów wewnętrznych. Należy upewnić się, że podczas docisku tkanki w planowanym miejscu mocowania, całkowita odległość od powierzchni tkanki do znajdujących się poniżej struktur była większa niż długość elementu mocującego CapSure™.
Należy uważać, aby nie użyć nadmiernego nacisku, ponieważ może to spowodować uszkodzenie tkanki, mocowanego materiału i/lub urządzenia.
Jeśli urządzenie zablokuje się i nie można go oddzielić od elementu mocującego, który został osadzony w siatce i/lub tkance, należy obrócić urządzenie w kierunku przeciwnym do ruchu wskazówek zegara, aby odłączyć element mocujący od tkanki i/lub uwolnić urządzenie. Jeśli element mocujący nie rozpręży się prawidłowo, należy wyjąć wyrób z ciała pacjenta i przetestować rozprężanie elementu mocującego nad gazą. Jeśli nie rozpręża się prawidłowo, należy wyrzucić urządzenie w odpowiedni sposób i użyć nowego systemu mocowania CapSure™. Po potwierdzeniu prawidłowego rozprężenia urządzenia do mocowania, można je ponownie włożyć w ciało pacjenta.
Bezpieczeństwo i skuteczność systemu stałego mocowania CapSure™ nie zostały zbadane u kobiet w ciąży lub karmiących piersią.
Produkt zawiera następujące substancje zdefiniowane jako CMR 1B w stężeniu powyżej 0,1% wagowo: kobalt, nr CAS 7440-48-4; nr WE 231-158-0. Aktualne dowody naukowe potwierdzają, że produkty medyczne wytwarzane ze stopów stali nierdzewnej zawierających kobalt nie powodują zwiększonego ryzyka zachorowania na raka ani nie mają negatywnego wpływu na rozrodczość. Aby uzyskać więcej informacji, należy odwiedzić stronę internetową ECHA: Strona internetowa - ECHA
Działania niepożądane
Działania niepożądane i potencjalne powikłania związane z działaniem produktów do mocowania, takich jak system do trwałego mocowania CapSure™, mogą obejmować między innymi: krwotok, ból, obrzęk i rumień w miejscu rany; posocznica/zakażenie; nawrót przepukliny/rozejście się rany, nadżerka i odpowiedź alergiczna u pacjentów ze stwierdzoną nadwrażliwością na PEEK i metale zawarte w stali nierdzewnej 316L, w tym chrom, nikiel, miedź i żelazo.