Covera™
Stent vascular recubierto
El ÚNICO stent recubierto indicado para injertos AV y fístulas AV nativas***
- Información general
- Experiencia clínica
- Instrucciones de uso electrónicas y recursos
Stent recubierto a medida para pacientes AV
El stent vascular recubierto Covera™ se basa en tecnologías probadas del líder en accesos AV. Esta plataforma de stent recubierto está diseñada para equilibrar la flexibilidad y la resistencia necesarias para abordar lesiones difíciles, desde el arco cefálico terminal, pasando por los segmentos basilicales del punto de giro, hasta la anastomosis venosa del injerto AV. Las configuraciones ensanchada y recta permiten un dimensionamiento y una adaptación precisos a la pared del vaso, mientras que el sencillo sistema introductor de ruedecilla con dos opciones de velocidad controla la colocación.
El stent vascular recubierto Covera™ ofreció resultados eficaces en dos ensayos clínicos distintos, uno para pacientes en diálisis con injertos AV y otro para pacientes en diálisis con fístulas AV.1
Flexibilidad y resistencia radial
Arquitectura única y flexible de la base del stent diseñada para adaptarse al vaso nativo en anatomías AV complejas.

- 1
- 2
- 3
- 4
- 5
Bordes contorneados diseñados para optimizar la aposición de las paredes y favorecer el flujo laminar
Carbono impregnado en toda la luz
Diseñado para la flexión, compresión y torsión, con puntales helicoidales y puentes en ángulo
Encapsulación completa entre dos capas de PTFEe diseñadas para resistir la hiperplasia neointimal en el área de tratamiento
Marcadores de tantalio para mejorar la visibilidad bajo radioscopia

- La configuración ensanchada está indicada en anatomías en las que el diámetro del vaso de salida es mayor que el de entrada
- La configuración recta está indicada en anatomías en las que el diámetro del vaso de salida es igual o menor que el de entrada

Punta atraumática diseñada para facilitar la inserción y extracción en el punto de acceso
Facilita un control preciso de la colocación
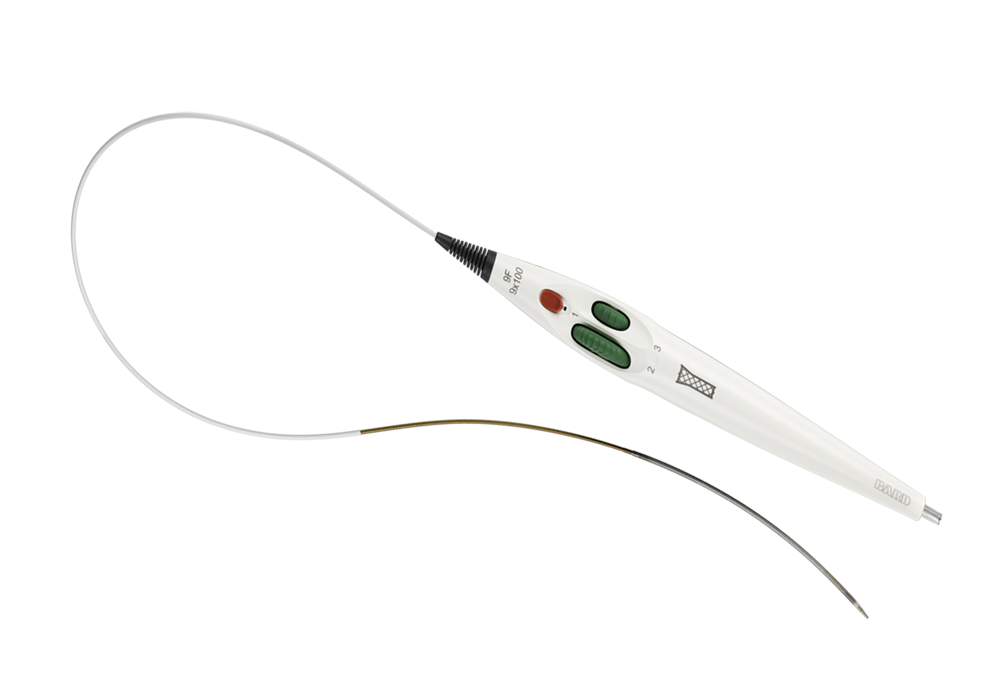
Sistema introductor triaxial intuitivo diseñado para realizar una colocación precisa y facilitar una cobertura óptima de la lesión
- 1
- 2
- 3
Vaina de estabilidad que permite una colocación suave y precisa
Ruedecilla de doble velocidad para control del operador
Agarre ergonómico que permite el despliegue con una sola mano
*** En EE. UU., a partir de enero de 2023.
1 Dolmatch B, Waheed U, Balamuthusamy S, Hoggard J, Settlage R; AVeVA Trial Investigators. Prospective, Multicenter Clinical Study of the Covera Vascular Covered Stent in the Treatment of Stenosis at the Graft-Vein Anastomosis of Dysfunctional Hemodialysis Access Grafts. J Vasc Interv Radiol. 2022;33(5):479-488.e3. doi:10.1016/j. jvir.2022.02.008. Datos en archivo del estudio clínico AVeNEW. A los 6 meses del ensayo AVeVA, la permeabilidad primaria de la lesión diana (TLPP) fue del 70,3 % (análisis proporcional). A los 6 meses del ensayo AVeNEW, la TLPP fue del 78,7 % para el stent vascular recubierto Covera™ frente al 47,9 % para solo ATP, con P < 0,001. 130 de los 142 (91,5 %) sujetos aleatorizados en el grupo del stent vascular Covera™ y 123 de los 138 (89,1 %) aleatorizados en el grupo de ATP terminaron su seguimiento a los 6 meses. La TLPP se define como el intervalo después de la intervención inicial hasta la siguiente reintervención de tipo clínico en el lugar de tratamiento original o adyacente a él, o hasta que la extremidad se abandona para el acceso permanente. En AVeNEW se proporciona la TLPP a los 6 meses (análisis de subgrupos) como datos observacionales sin valores P. En AVeNEW, los pacientes que recibieron el stent vascular recubierto Covera™ tuvieron 103 reintervenciones que implicaban una nueva lesión, en comparación con las 72 reintervenciones en el grupo de solo ATP a los 24 meses. A los 30 días, la ausencia de acontecimientos de seguridad primarios fue del 96,4 % en AVeVA y del 95,0 % (stent vascular recubierto Covera™) frente al 96,4 % (solo ATP) en AVeNEW (P < 0,0022). La ausencia de acontecimientos de seguridad primarios se definió como la ausencia de episodios adversos relacionados con el circuito de acceso que requirieran otra intervención, cirugía u hospitalización, o que provocaran la muerte.
Consulte las instrucciones de uso para conocer las indicaciones de uso, las contraindicaciones, las advertencias, las precauciones, las complicaciones, los acontecimientos adversos e información de seguridad detallada del producto.
BD-23522v2
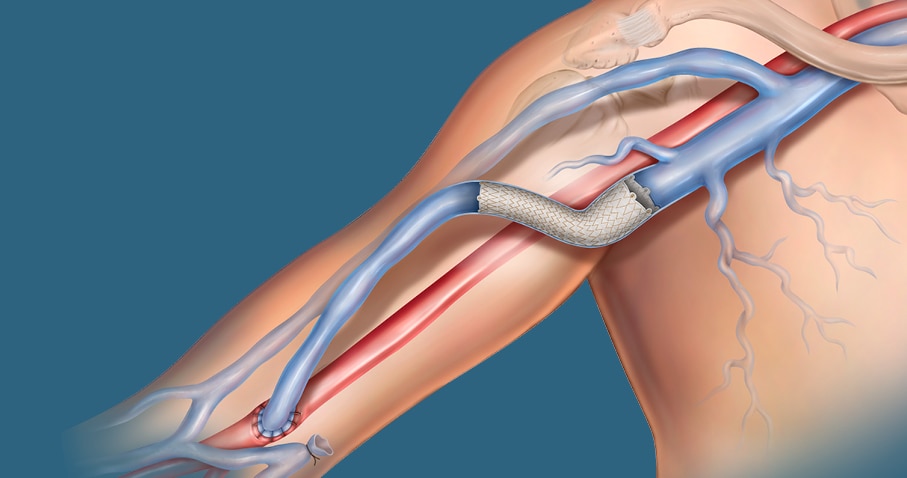
El stent vascular recubierto Covera™ ha sido diseñado para abordar lesiones complejas dentro del circuito de acceso AV, incluyendo el arco cefálico terminal, los segmentos basilicales del punto de giro y la anastomosis del injerto venoso.
El stent vascular recubierto Covera™ ofreció resultados eficaces en dos ensayos clínicos distintos, uno para pacientes en diálisis con injertos AV y otro para pacientes en diálisis con fístulas AV; en ambos ensayos demostró las ventajas de su innovador diseño.1
AVeVA fue un estudio prospectivo, no aleatorizado, multicéntrico de un solo grupo del stent vascular recubierto Covera™ utilizado para tratar la estenosis en la anastomosis de un injerto arteriovenoso y de la vena de salida. 110 pacientes recibieron tratamiento con el stent vascular recubierto Covera™ en 14 centros de investigación de EE. UU.
El estudio clínico AVeVA demostró que el stent vascular recubierto Covera™ es eficaz para tratar la estenosis en la anastomosis del injerto venoso de pacientes que se someten a diálisis con un injerto AV.
| Diseño del estudio | Prospectivo, no aleatorizado, multicéntrico, de un solo grupo |
| Objetivo | Evaluar la seguridad y eficacia del stent vascular recubierto Covera™ para tratar lesiones estenóticas en la anastomosis del injerto venoso de pacientes en hemodiálisis que se someten a diálisis con un injerto AV. |
| Estado | Seguimiento de 24 meses completado |
| Número de pacientes/centros | 110 pacientes recibieron tratamiento con el stent vascular recubierto Covera™ en 14 centros de investigación de EE. UU. |
| Criterio de valoración principal de la eficacia | Permeabilidad primaria de la lesión diana (TLPP): 6 meses |
| Criterio de valoración principal de la seguridad | La ausencia de acontecimientos adversos relacionados con el circuito de acceso que requirieran otra intervención, cirugía u hospitalización, o que provocaran la muerte en un plazo de 30 días. |
| Seguimiento | 30 y 90 días; 6, 12, 18 y 24 meses |
Permeabilidad primaria de la lesión diana (TLPP) a los 6 meses tras tratar la estenosis anastomótica del injerto AV con injertos de stent BD
Este cuadro solo tiene fines educativos y no pretende comparar. Las diferencias en el diseño del estudio pueden afectar a los resultados. Consulte los manuscritos completos para obtener todos los detalles del diseño del estudio.
En el estudio clínico AVeVA, el stent vascular recubierto Covera™ se estudió en una cohorte de pacientes difíciles.
| Diseño del estudio | Prospectivo, multicéntrico, aleatorizado y controlado simultáneamente |
| Objetivo | Evaluar la seguridad y eficacia del stent vascular recubierto Covera™ para tratar lesiones estenóticas en la salida venosa de la extremidad superior del circuito de acceso AV de pacientes en hemodiálisis que se someten a diálisis con una fístula AV. |
| Estado | Seguimiento de 24 meses completado |
| Número de pacientes/centros | 280 sujetos aleatorizados en 24 centros de investigación (EE. UU., UE y ANZ) |
| Criterio de valoración principal de la eficacia | Permeabilidad primaria de la lesión diana (TLPP): 6 meses |
| Criterio de valoración principal de la seguridad | Ausencia de acontecimientos de seguridad graves definidos por el protocolo que afecten al circuito de acceso AV en un plazo de 30 días |
| Seguimiento | Alta del hospital; 30 y 90 días; 6, 12, 18 y 24 meses |
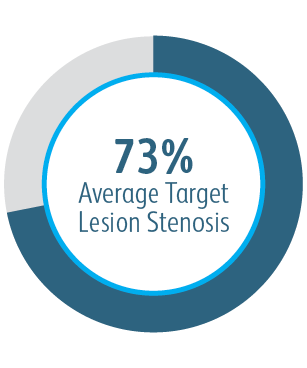
En el estudio clínico AVeNEW, el stent vascular recubierto Covera™ se utilizó para tratar a una población de pacientes complicada con características de lesión difíciles.
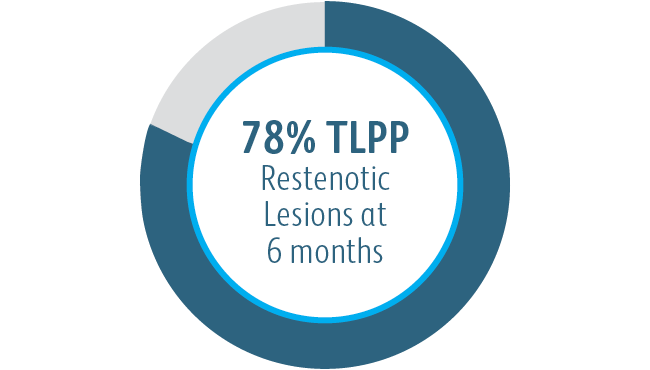
El stent vascular recubierto Covera™ fue superior al control de ATP a los 6 y 12 meses en lo que respecta a la TLPP para tratar la estenosis del flujo de salida venoso en pacientes sometidos a diálisis con una fístula arteriovenosa.
Todos los subgrupos mostraron beneficios a los 6 meses
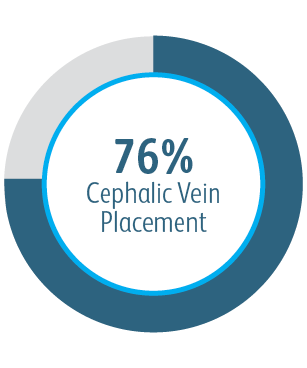
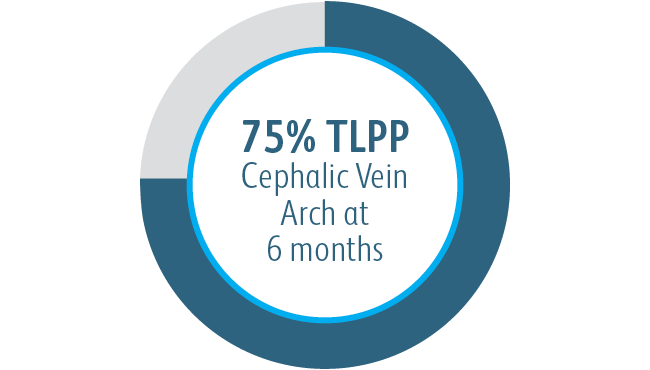
En todos los subgrupos de localización de la lesión diana analizados, el stent vascular recubierto Covera™ demostró una permeabilidad primaria de la lesión diana mayor que solo ATP, incluidos los pacientes tratados en el arco de la vena cefálica.
Otros criterios de valoración del estudio clínico AVeNEW
Más allá de los beneficios de la permeabilidad primaria de la lesión diana, el stent vascular recubierto Covera™ demostró un alto grado de éxito técnico agudo y amplió el tiempo medio entre intervenciones de la lesión diana en comparación con solo ATP.
En el estudio clínico AVeNEW, 77 pacientes con estenosis del arco de la vena cefálica recibieron tratamiento con el
stent vascular recubierto Covera™.
En este ejemplo de caso se presenta la angiografía inicial que muestra el estrechamiento de los vasos y el éxito técnico agudo con la restauración del vaso y la adaptabilidad del stent recubierto.
* Haskal ZJ, Trerotola S, Dolmatch B, et al. Stent graft versus balloon angioplasty for failing dialysis-access grafts. N Engl J Med. 2010 Feb 11;362(6):494-503.
** Haskal ZJ, Saad TF, Hoggard JG, et al. Prospective, randomized, concurrently-controlled study of a stent graft versus balloon angioplasty for treatment of arteriovenous access graft stenosis: 2-year results of the RENOVA study. J Vasc Interv Radiol. 2016 Aug;27(8):1105-1114.e3.
*** En EE. UU. a partir de noviembre de 2022.
1 Dolmatch B, Waheed U, Balamuthusamy S, Hoggard J, Settlage R; AVeVA Trial Investigators. Prospective, multicenter clinical study of the Covera Vascular Covered Stent in the treatment of stenosis at the graft-vein anastomosis of dysfunctional hemodialysis access grafts. J Vasc Interv Radiol. 2022;33(5):479-488.e3. doi:10.1016/j. jvir.2022.02.008. Datos en archivo del estudio clínico AVeNEW. A los 6 meses del ensayo AVeVA, la permeabilidad primaria de la lesión diana (TLPP) fue del 70,3 % (análisis proporcional). A los 6 meses del ensayo AVeNEW, la TLPP fue del 78,7 % para el stent vascular recubierto Covera™ frente al 47,9 % para solo ATP, con P < 0,001. 130 de los 142 (91,5 %) sujetos aleatorizados en el grupo del stent vascular Covera™ y 123 de los 138 (89,1 %) aleatorizados en el grupo de ATP terminaron su seguimiento a los 6 meses. La TLPP se define como el intervalo después de la intervención inicial hasta la siguiente reintervención de tipo clínico en el lugar de tratamiento original o adyacente a él, o hasta que la extremidad se abandona para el acceso permanente. En AVeNEW se proporciona la TLPP a los 6 meses (análisis de subgrupos) como datos observacionales sin valores P. En AVeNEW, los pacientes que recibieron el stent vascular recubierto Covera™ tuvieron 103 reintervenciones que implicaban una nueva lesión, en comparación con las 72 reintervenciones en el grupo de solo ATP a los 24 meses. A los 30 días, la ausencia de acontecimientos de seguridad primarios fue del 96,4 % en AVeVA y del 95,0 % (stent vascular recubierto Covera™) frente al 96,4 % (solo ATP) en AVeNEW (P < 0,0022). La ausencia de acontecimientos de seguridad primarios se definió como la ausencia de episodios adversos relacionados con el circuito de acceso que requirieran otra intervención, cirugía u hospitalización, o que provocaran la muerte.
2 El éxito técnico agudo se definió como el despliegue correcto del implante en la ubicación prevista evaluada en el momento de la intervención inicial, según la opinión del operador. Estudio clínico AVeNEW. Datos en archivo. Bard Peripheral Vascular Inc., Tempe, AZ.
3 El índice de función de permeabilidad de la lesión diana (IPF-T) se define como el tiempo transcurrido desde la intervención inicial del estudio hasta la finalización del estudio o el abandono total, dividido por el número de visitas para una nueva intervención realizada en la lesión diana con el fin de mantener el acceso vascular para hemodiálisis. IPF-T medio de 380,40 días con el stent vascular recubierto Covera™ frente a los 217,57 días con solo ATP a los 24 meses. Estudio clínico AVeNEW. Datos en archivo. Bard Peripheral Vascular Inc., Tempe, AZ.
Consulte las instrucciones de uso para conocer las indicaciones de uso, las contraindicaciones, las advertencias, las precauciones, las complicaciones, los acontecimientos adversos e información de seguridad detallada del producto.
BD-23522v2
En la bibliografía de BD se ofrece información que puede utilizar para continuar trabajando para alcanzar la excelencia.