Ballonnet à revêtement médicamenteux Lutonix™ Cathéter pour ATP
Ballonnets à revêtement médicamenteux pour angioplastie

- Présentation
- Caractéristiques
- Données cliniques
- Instructions d'utilisation et ressources
Le cathéter pour ATP à ballonnet recouvert de médicament Lutonix™ est proposé dans des configurations de guide de 0,018" et 0,035" pour le traitement des maladies artérielles périphériques dans les artères fémorales superficielles et poplitées. Le cathéter à ballonnet recouvert de médicament Lutonix™ administre une dose de 2 μg/mm2 de paclitaxel. Il est conçu pour offrir la polyvalence nécessaire au traitement de lésions de tailles et de longueurs variables.Il est conçu pour améliorer les procédures fémoro-poplitées. Il offre pour cela :
- Un grand choix de tailles de matrices
- Des indications étendues
- Résultats éprouvés dans le cadre d’un essai clinique de niveau 11

- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
Faible dose de médicament :
Dose optimale de médicament de 2 μg/mm2 du paclitaxel
Embout conique :
Conçu pour faciliter l’avancée du cathéter vers la région sténotique du vaisseau et à travers celle-ci.
Profil de gaine de petite taille :
5 F ou moins
Revêtement durable :
Conçu pour limiter l’écaillage du médicament lors de la préparation et de la manipulation
Ballonnet disponible dans des longueurs allant jusqu’à 300 mm sur les tailles sélectionnées de 0,018
Seul le ballonnet recouvert de médicament de 300 mm est disponible aux États-Unis2
Longueur de cathéter de 100 cm et 130 cm :
S’adapte à votre site d’accès préféré
Compatibilité avec les guides de 0,018 et 0,035 :
Pour soutenir votre algorithme de traitement
Le système de graduations GeoAlign™ est une règle standard non radio-opaque située sur le corps du cathéter conçue pour :
- Faciliter la mise en place répétée du cathéter
- Améliorer l’efficacité des procédures
1 Données archivées de l’essai clinique LEVANT 2. N = 476. À 12 mois, le traitement par Lutonix™ 035 a permis d’obtenir un taux de perméabilité primaire de 73,5 % contre 56,8 % avec l’ATP seule (p = 0,001). La perméabilité primaire est définie comme l’absence de resténose binaire définie par un PSVR DUS ≥ 2,5 et l’absence de revascularisation de la lésion cible (TLR). À 12 mois, le traitement par Lutonix™ 035 a permis d’obtenir un taux d’absence d’événement de sécurité primaire de 86,8 % contre 81,9 % avec l’ATP seule (p = 0,185). La sécurité primaire est définie comme l’absence de décès périopératoire toutes causes confondues et l’absence d’amputation (ATK ou BTK), de réintervention et de décès lié au membre de référence à 1 an. Les chiffres indiqués sont des analyses de Kaplan-Meier et non des données pré-spécifiées.
3 Les marqueurs GeoAlign™ ne remplacent pas la radioscopie. Lorsque le cathéter est exposé au système vasculaire, l’emplacement du ballonnet doit être confirmé sous guidage radioscopique de haute qualité. Une étude chez les animaux (ATP répétée dans l’artère porcine) a été réalisée par trois médecins qui ont testé le cathéter à ballonnet recouvert de médicament Lutonix™ 035 (sans médicament) et le cathéter Ultraverse™ 035 pour ATP, tous deux avec des marqueurs GeoAlign™, par rapport à l’angioplastie conventionnelle par ballonnet sans marqueurs GeoAlign™ (n = 112, test n = 96, contrôle n = 16). Données sur les animaux archivées. Les résultats des tests réalisés sur les animaux par BD ne sont pas forcément indicatifs de la performance clinique réelle. Différentes méthodes de test peuvent produire des résultats différents.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité. Sur ordonnance uniquement
BD-38946
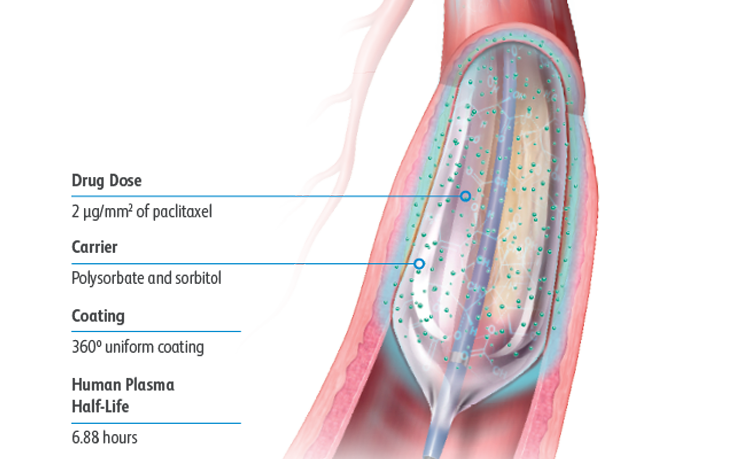
La formulation du ballonnet recouvert de médicament Lutonix™ a été conçue pour offrir un équilibre optimal entre sécurité et efficacité avec une dose de 2 μg/mm2 et des excipients polysorbate et sorbitol qui, ensemble, permettent un transfert efficace du médicament vers la paroi vasculaire.
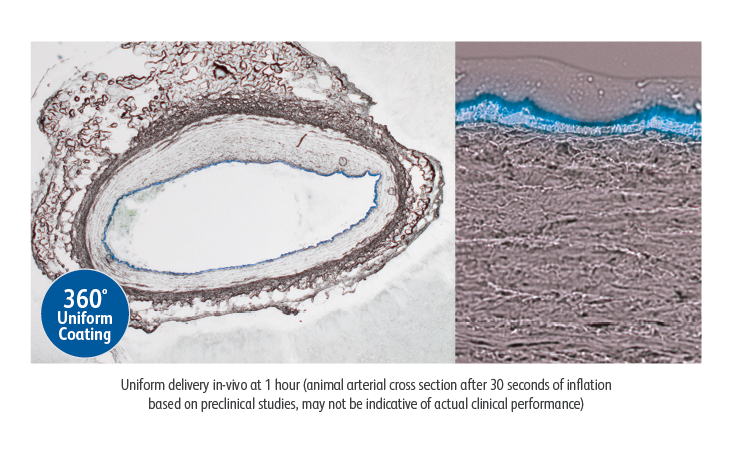
Le ballonnet recouvert de médicament Lutonix™ 035 a permis d’obtenir un revêtement homogène, ce qui s’est traduit par :
- un revêtement à 360° de paclitaxel au niveau du vaisseau cible1
- une épaisseur de revêtement d’environ 6,46 μm1

La formulation du revêtement du ballonnet recouvert de médicament Lutonix™ 035 est conçue pour :
- Assurer l’absorption rapide du médicament au niveau de la paroi du vaisseau pendant le gonflage
- Administrer de manière uniforme le médicament au niveau de la paroi du vaisseau
- Aider à réduire l’exposition inutile du personnel et des patients aux médicaments
Lors d’un test d’agitation à sec, le ballonnet recouvert de médicament Lutonix™ 035 a montré une perte de médicament < 0,1 %.2
Les données issues d’une étude préclinique sur les animaux ont montré que le ballonnet recouvert de médicament Lutonix™ présentait les niveaux pharmacologiques souhaités avec des effets biologiques sans signe d’embolie en aval importante ou de toxicité systémique.3
1 Données archivées du banc d’essai et de l’étude préclinique sur les animaux. Les résultats du banc d’essai et les données précliniques ne sont pas forcément indicatifs de la performance clinique réelle. Différentes méthodes de test peuvent produire des résultats différents.
2 Données des tests au banc de gonflage/d’agitation à sec archivées, BD, Tempe AZ. L’essai d’agitation a permis de mesurer la teneur moyenne en médicament perdue après le gonflage du ballon et après avoir légèrement frappé le dispositif contre les parois d’un tube à centrifuger, à gauche et à droite, à cinq reprises. n = 5. Les résultats des bancs d’essai ne sont pas forcément indicatifs de la performance clinique réelle. Différentes méthodes de test peuvent produire des résultats différents.
3 Étude de Virmani sur les données animales précliniques et les bonnes pratiques de laboratoire (BPL). Données précliniques archivées. Les résultats précliniques ne sont pas forcément indicatifs de la performance clinique réelle. Différentes méthodes de test peuvent produire des résultats différents.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité. Sur ordonnance uniquement
BD-38946
Le registre mondial de Lutonix a montré une efficacité soutenue du ballonnet recouvert de médicament Lutonix™ 035 au sein d’une population hétérogène de patients dans la pratique clinique réelle.1
Le critère d’évaluation principal de l’efficacité a été mesuré par l’absence de revascularisation de la lésion cible selon la méthode Kaplan-Meier (KM). Il s’est révélé être de 94,1 % à 12 mois et de 90,3 % à 24 mois.1
L’efficacité du ballonnet recouvert de médicament Lutonix™ 035 a été maintenue dans les sous-groupes lésions longues et resténose intra-endoprothèse de 88,2 % et 84,6 % d’absence de revascularisation de la lésion cible à 24 mois, respectivementt.1
L’étude pivot LEVANT 2 est une étude prospective mondiale, randomisée, en simple aveugle, menée dans 54 centres (42 centres aux États-Unis et 12 en Europe), qui a recruté tous les patients selon un protocole unique, en vue de comparer le ballonnet recouvert de médicament Lutonix™ 035 à l’ATP standard.2
L’étude a atteint ses critères d’évaluation principaux en termes de sécurité et d’efficacité.
- Sécurité : Le ballonnet recouvert de médicament Lutonix™ 035 a démontré un profil de sécurité similaire à l’ATP
- Efficacité : Le ballonnet recouvert de médicament Lutonix™ 035 a montré un taux de perméabilité primaire supérieur de 29,4 % à 12 mois par rapport à l’ATP
1 Lutonix Global SFA Real-World Registry, n = 691. Le critère d’évaluation principal de la sécurité était l’absence de réintervention dans le vaisseau cible, de taux majeur d’amputation du membre et de décès lié au dispositif ou à la procédure à 30 jours. L’absence d’événements de sécurité primaires à 30 jours était de 99,4 % (681/681). Le critère d’évaluation principal de l’efficacité est défini comme l’absence de revascularisation de la lésion cible à 12 mois. Le taux d’absence de revascularisation de la lésion cible par sujet à 12 mois était de 93,4 % (605/648). L’estimation de la survie avec absence de revascularisation de la lésion cible de Kaplan-Meier était de 94,1 %. Les lésions longues ont été définies comme toute lésion >= 140 mm. Tous les sujets traités avec le ballonnet recouvert de médicament Lutonix™ 035. Durant l’essai clinique LEVANT 2 IDE, le traitement à l’aide du ballonnet recouvert de médicament Lutonix™ 035 a permis d’obtenir un taux d’absence de revascularisation de la lésion cible de 87,7 % à 12 mois (250/285) et de 82,0 % à 24 mois. Données archivées, Becton, Dickinson and Company.
2 Données archivées de l’essai clinique LEVANT 2. N = 476. À 12 mois, le traitement par Lutonix™ 035 a permis d’obtenir un taux de perméabilité primaire de 73,5 % contre 56,8 % avec l’ATP seule (p = 0,001). La perméabilité primaire est définie comme l’absence de resténose binaire définie par un PSVR DUS ≥ 2,5 et l’absence de revascularisation de la lésion cible (TLR). À 12 mois, le traitement par Lutonix™ 035 a permis d’obtenir un taux d’absence d’événement de sécurité primaire de 86,8 % contre 81,9 % avec l’ATP seule (p = 0,185). La sécurité primaire est définie comme l’absence de décès périopératoire toutes causes confondues (<= 30 jours) et l’absence d’amputation (ATK ou BTK), de réintervention et de décès lié au membre de référence à 1 an. Les chiffres indiqués sont des analyses de Kaplan-Meier et non des données pré-spécifiées.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité. Sur ordonnance uniquement
BD-38946
BD vous propose une bibliothèque de documents pour le domaine de l’industrie.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité. Sur ordonnance uniquement
BD-38946