Veuillez noter que certains produits, services ou caractéristiques peuvent ne pas être disponibles dans votre région. Veuillez consulter votre représentant BD local.
Indications
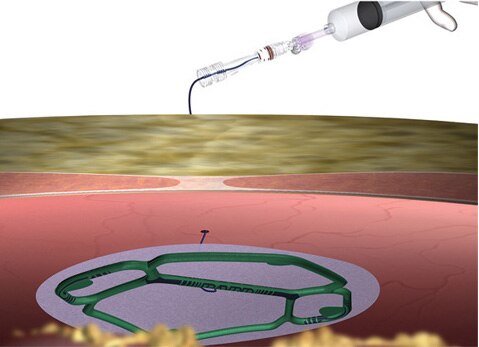
La maille Ventralight™ ST est indiquée pour la reconstruction d’anomalies des tissus mous, comme dans la réparation d’une hernie ventrale, incisionnelle et ombilicale. Le système de positionnement Echo PS™ est conçu pour faciliter l’installation de la maille Ventralight™ ST dans le cadre de réparations de hernies par laparoscopie.
Contre-indications
- N’utilisez pas la maille chez les nourrissons, les enfants ou les femmes enceintes ; leur croissance pourrait être compromise par l’utilisation de ce type de matériau de maille.
- L’utilisation de cette maille chez les femmes enceintes ou qui allaitent n’a pas été évaluée.
- N’utilisez pas cette maille pour la reconstruction d’anomalies cardiovasculaires.
- Selon la littérature, des adhérences peuvent se former si le polypropylène est placé en contact direct avec l’intestin ou les viscères.
Avertissements
- L’utilisation d’une maille permanente sur une blessure contaminée ou infectée peut entraîner une infection, la formation de fistules et/ou l’extrusion de la maille.
- En cas d’infection, un traitement agressif s’impose. Le retrait de la maille doit également être envisagé. Une infection non traitée peut nécessiter le retrait de la maille.
- Si la maille inutilisée est entrée en contact avec des instruments ou des consommables utilisés sur un patient ou si elle a été contaminée par des fluides organiques, éliminez-la soigneusement afin d’éviter tout risque de transmission d’infections virales ou autres.
- Pour prévenir toute récidive lors de la réparation d’une hernie, la maille doit être suffisamment grande pour dépasser des bords de la zone de l’anomalie, en tenant compte de tout facteur clinique supplémentaire propre au patient. Il convient de porter une grande attention au positionnement et à l’espacement de la fixation de la maille afin d’éviter toute tension excessive ou formation d’un espace entre la maille et le tissu fascial.
- Le dispositif est fourni stérile. Inspectez l’emballage pour vérifier qu’il est intact et non endommagé avant utilisation.
- Ce dispositif est à usage unique. La réutilisation, le retraitement, la restérilisation et/ou le reconditionnement pourraient compromettre l’intégrité structurelle et/ou les principales caractéristiques conceptuelles ou matérielles, essentielles aux performances générales du dispositif, et entraîner un dysfonctionnement de ce dernier, causant potentiellement des blessures au patient. La réutilisation, le retraitement, la restérilisation ou le reconditionnement pourraient également générer un risque de contamination du dispositif et/ou entraîner une infection ou une infection croisée chez le patient, notamment la transmission de maladies infectieuses d’un patient à un autre. La contamination du dispositif peut entraîner des lésions, des maladies ou le décès du patient ou de l’utilisateur final.
- La maille doit être utilisée dès que le sachet extérieur en aluminium a été ouvert. Ne le conservez pas en vue d’une utilisation ultérieure. Éliminez les parties inutilisées de la maille.
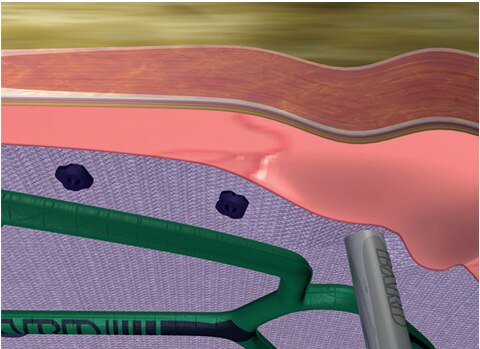
- Veillez à son orientation correcte ; le côté enduit de la maille doit être orienté contre l’intestin ou les organes sensibles. Ne placez pas le côté polypropylène contre l’intestin. Des adhérences peuvent se former si le côté polypropylène est placé en contact direct avec l’intestin ou les viscères (voir la section Orientation de surface).
- N’appliquez pas d’outils tranchants, émettant de la chaleur ou ultrasons (tels que des ciseaux, des aiguilles, des agrafes, des outils diathermiques, etc.) sur le système de positionnement Echo PS™.
- Le système de positionnement Echo PS™ ne doit pas être utilisé avec d’autres mailles pour hernie que celles avec lesquelles il est livré/auxquelles il est préfixé.
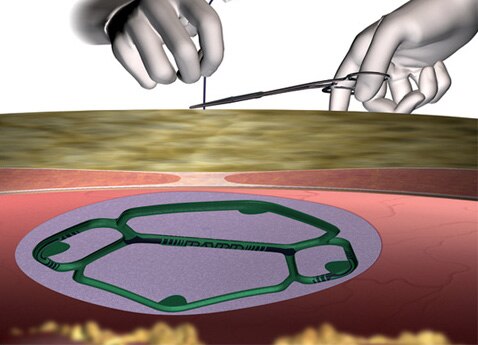
- La maille Ventralight™ ST est le seul implant permanent du dispositif. L’adaptateur de gonflage et la seringue doivent être maintenus à l’extérieur du patient et jetés après usage. Le système de positionnement Echo PS™ (comprenant le ballonnet, tous les connecteurs et le tube de gonflage) doit être retiré du patient et éliminé de manière adéquate. Il ne fait pas partie de l’implant permanent.
- Éliminez l’outil d’introduction et tous les composants du système de positionnement Echo PS™ (y compris la seringue et l’adaptateur de gonflage) après utilisation. Ce produit peut présenter un risque biologique. La manipulation et l’élimination doivent s’effectuer conformément aux pratiques médicales acceptées et aux réglementations locales et nationales en vigueur.
- Cette maille n’est pas conçue pour la réparation du prolapsus des organes pelviens par voie transvaginale.
- Cette maille n’est pas conçue pour le traitement de l’incontinence urinaire à l’effort.
Précautions
- Lisez l’intégralité des instructions avant utilisation.
- Seuls les médecins dûment formés aux techniques chirurgicales appropriées peuvent utiliser ce dispositif.
- La sécurité et l’efficacité de la maille Ventralight™ ST avec système de positionnement Echo PS™ en présence de tumeurs malignes dans la cavité abdomino-pelvienne n’ont pas été évaluées dans le cadre d’essais cliniques.
- La visualisation doit être préservée tout au long de l’intervention chirurgicale. En outre, le retrait du système de positionnement Echo PS™ sous laparoscopie nécessite une visualisation suffisante de l’ensemble du dispositif et de l’anatomie voisine pour permettre son retrait adéquat.
- Ne coupez pas la maille. Cela affecterait l’interface entre la maille et le système de positionnement.
Réactions indésirables
- Les complications possibles peuvent notamment inclure sérome, adhérence, hématome, douleur, infection, inflammation, extrusion, érosion, migration, formation de fistules, réaction allergique et récidive de la hernie ou de l’anomalie des tissus mous. Veuillez consulter la notice de l’emballage pour en savoir plus sur les informations de sécurité et le mode d’emploi.
Références
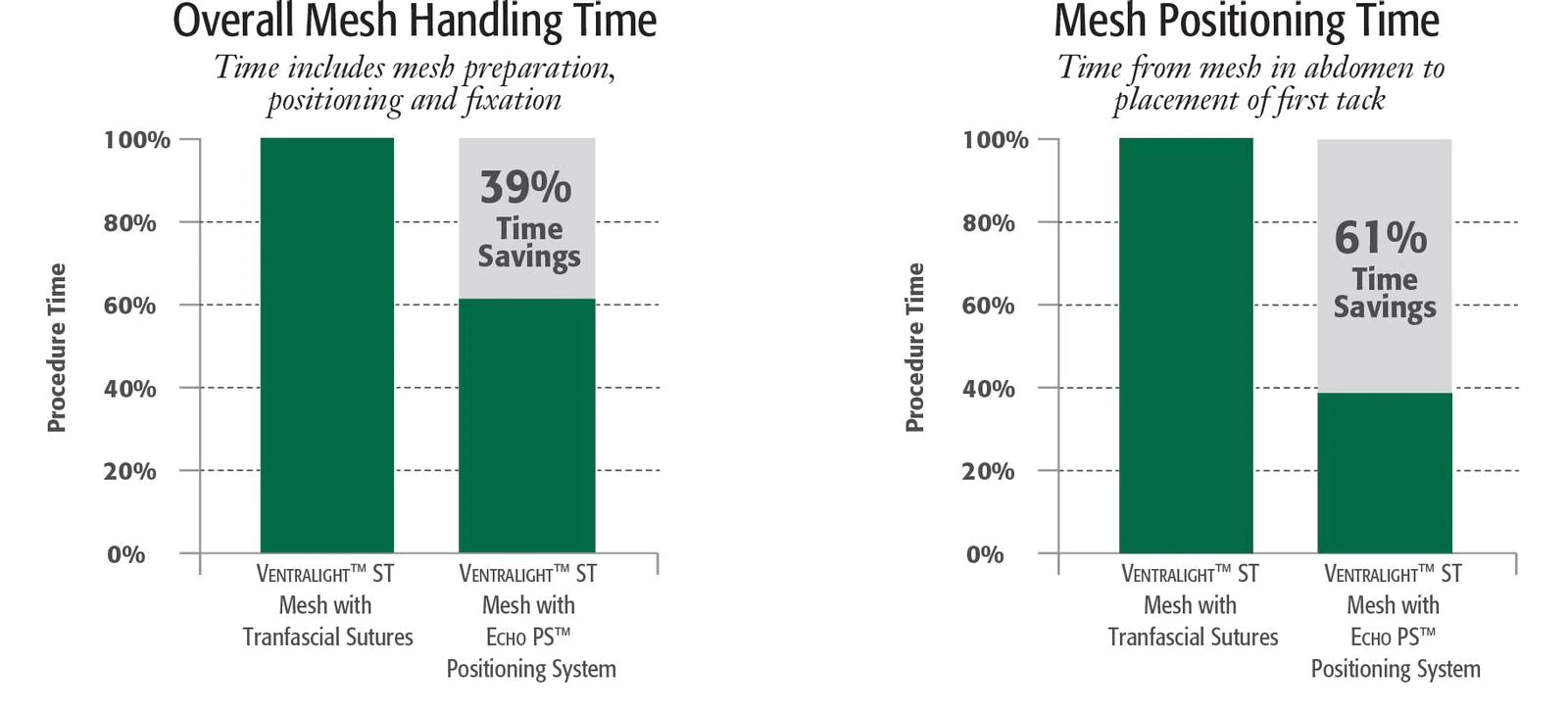
- Par comparaison avec le positionnement avec des sutures transfasciales dans le cadre d’une étude préclinique.
- Données archivées chez C. R. Bard, Inc. Il est possible que les résultats ne correspondent pas aux performances chez l’homme.