Referencias
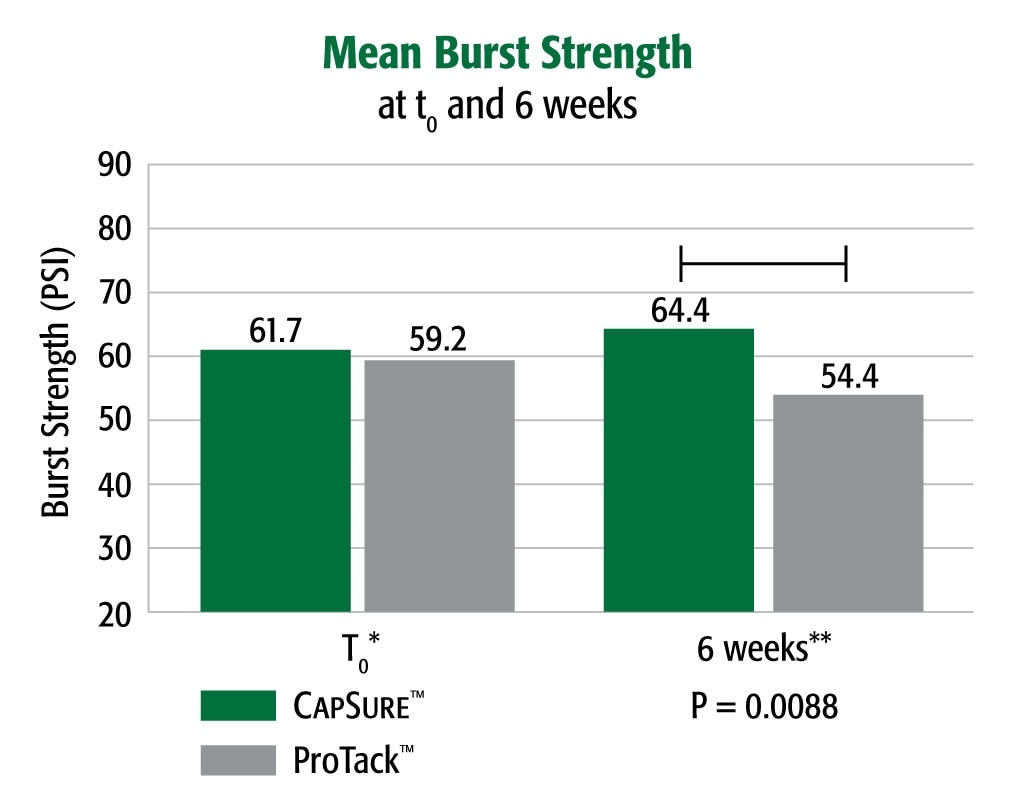
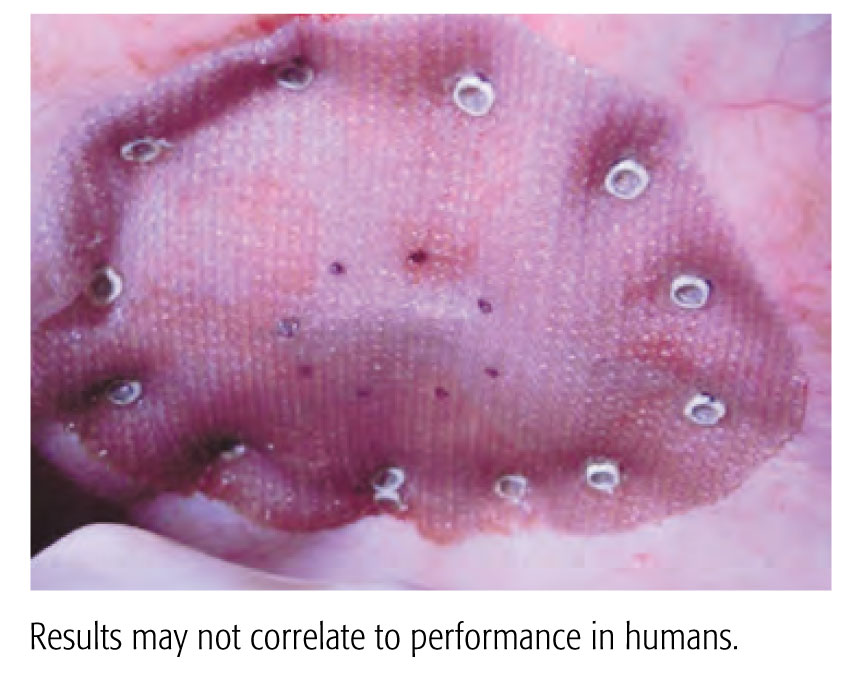
Datos de referencia. Es posible que los resultados no se correlacionen con el rendimiento en humanos.
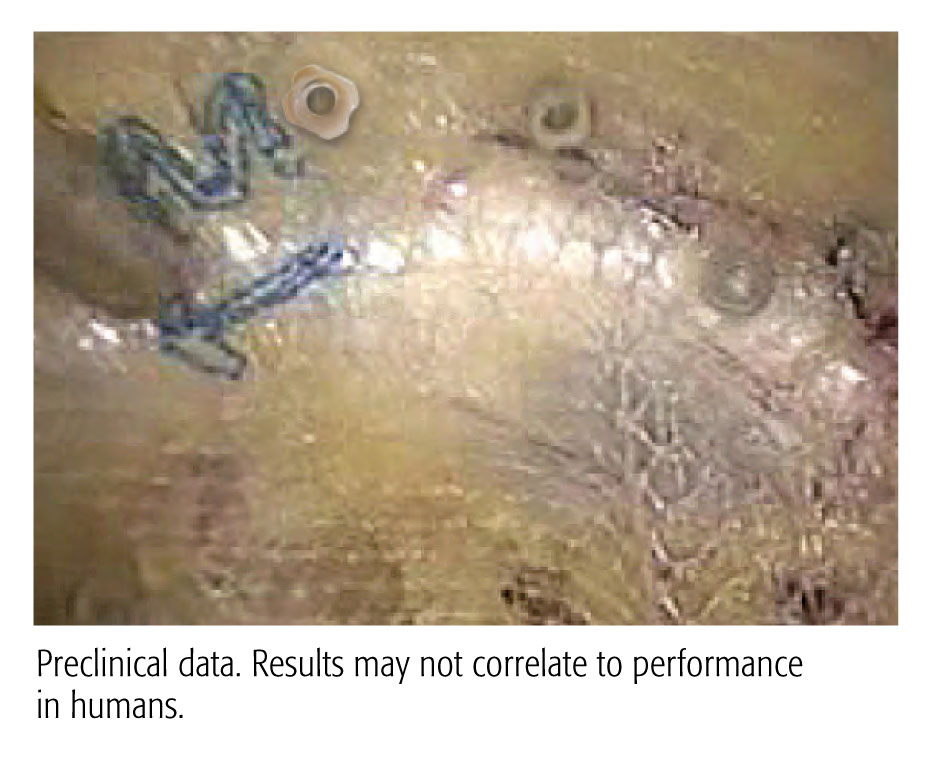
Datos preclínicos. Es posible que los resultados no se correlacionen con el rendimiento en humanos
Descargos de responsabilidad
Es posible que no todos los productos, servicios, reclamos o características de los productos estén disponibles o sean válidos en su área local. Consulte con su representante local de BD.
Consulte en las etiquetas e instrucciones de uso de los productos las indicaciones, contraindicaciones, peligros, advertencias y precauciones.
Indicaciones
El sistema de fijación permanente CapSure™ está indicado para la aproximación de tejido blando y la fijación de mallas quirúrgicas a tejidos durante las intervenciones quirúrgicas laparoscópicas en la reparación de hernias ventrales e inguinales.
Contraindicaciones
Este dispositivo no está destinado para un uso distinto del indicado.
No utilice el dispositivo si no puede confirmarse visualmente la hemostasia tras la aplicación.
Se aplican las contraindicaciones asociadas a los procedimientos quirúrgicos laparoscópicos relacionados con la fijación de mallas, incluidas, entre otras, la fijación de estructuras vasculares o neuronales o en tejidos isquémicos o necróticos.
Inspeccione detenidamente el área que rodea el tejido que debe fijarse para evitar la penetración accidental en estructuras subyacentes como huesos, nervios, vasos y vísceras. El uso del sistema de fijación permanente CapSure™ está contraindicado cerca de tales estructuras. A modo de referencia, la longitud del fijador debajo de su cabezal es de 3,2 mm y el cabezal del fijador mide 1 mm más (4,2 mm en total).
Este dispositivo no debe usarse en tejidos con una relación anatómica directa con estructuras vasculares o nerviosas principales. Esto incluye la introducción de fijadores en el diafragma cerca del pericardio, la aorta o la vena cava inferior en reparaciones de hernias diafragmáticas.
Advertencias
El sistema de fijación permanente CapSure™ está diseñado únicamente para un solo uso. NO VUELVA A ESTERILIZAR. La reutilización, el reprocesamiento, la reesterilización o el reenvasado podrían afectar a la integridad estructural o a las características esenciales de los materiales y del diseño, que son fundamentales para el funcionamiento general del dispositivo y pueden provocar fallos en el dispositivo que pueden causar lesiones al paciente. La reutilización, el reprocesamiento, la reesterilización o el reenvasado también pueden crear un riesgo de contaminación del dispositivo o causar infección o infección cruzada en el paciente, entre otras, la transmisión de enfermedades infecciosas de un paciente a otro. La contaminación del dispositivo podría provocar lesiones, enfermedades o el fallecimiento del paciente o del usuario final.
No use después de la fecha de vencimiento del envase.
Este producto se suministra estéril. Inspeccione el envase para asegurarse de que está intacto y sin daños antes de utilizarlo.
Verifique la compatibilidad mecánica y eléctrica de los dispositivos de diferentes fabricantes antes de utilizarlos juntos en un procedimiento.
Se debe evaluar la compatibilidad de las prótesis antes de su uso.
Los usuarios deben estar familiarizados con los procedimientos y técnicas quirúrgicos que utilizan materiales permanentes antes de emplear los fijadores del sistema de fijación permanente CapSure™ para el cierre de heridas, ya que el riesgo de dehiscencia de la herida puede variar según el lugar de aplicación y el material utilizado.
Tal como ocurre con cualquier material de implante, la presencia de contaminación bacteriana puede aumentar la capacidad infecciosa de las bacterias. Debe seguirse la práctica quirúrgica aceptada con respecto al drenaje y cierre de heridas infectadas o contaminadas. Después de su uso, el sistema de fijación permanente CapSure™ podría ser un riesgo biológico potencial. Manipule y deseche de acuerdo con las leyes locales y federales relativas a los residuos médicos.
Precauciones
Lea todas las instrucciones antes de usar el sistema de fijación permanente CapSure™.
Las intervenciones quirúrgicas deben realizarse únicamente a través de profesionales formados que conozcan adecuadamente las técnicas quirúrgicas pertinentes. Consulte en la literatura médica la técnica, las complicaciones y los riesgos antes de realizar una intervención quirúrgica.
El sistema de fijación permanente CapSure™ puede usarse con la mayoría de los trocares de 5 mm. Inserte el dispositivo en el trocar antes de introducirlo en el paciente para asegurarse de la compatibilidad. El sistema de fijación permanente CapSure™ debe poder introducirse y extraerse del trocar con facilidad y sin aplicar demasiada fuerza. Si emplea demasiada fuerza, podría dañar el instrumento.
Debe aplicarse una presión contraria adecuada en la región objetivo. Evite colocar directamente la mano o el dedo sobre el lugar de implementación del fijador para evitar daños.
Tenga precaución al aplicar el fijador CapSure™ en huesos, vasos, nervios o vísceras subyacentes. El lugar de fijación previsto debe evaluarse para garantizar que, al comprimir el tejido, la distancia total desde la superficie de él a cualquier estructura subyacente sea mayor que la longitud del fijador CapSure™.
Debe tener cuidado de no ejercer demasiada presión contraria, ya que podría dañar el tejido, el material que se va a fijar o el dispositivo.
Si el dispositivo se bloquea y no puede separarse de un fijador que se haya introducido en la malla o el tejido, gire el dispositivo de derecha a izquierda para liberar el fijador del tejido o el dispositivo. Si el fijador no se coloca correctamente, retire el dispositivo del paciente y pruébelo en una gasa para garantizar que se fije bien; de lo contrario, deseche el dispositivo adecuadamente y utilice un nuevo sistema de fijación permanente CapSure™. Cuando confirme que se fija de forma correcta, puede volver a introducir el dispositivo en el paciente.
No se han evaluado ni establecido la seguridad y la eficacia del sistema de fijación permanente CapSure™ en mujeres embarazadas o lactantes.
Este dispositivo contiene las siguientes sustancias definidas como CMR 1B en una concentración superior al 0,1 % peso por peso: cobalto; n.° CAS 7440-48-4; n.° EC 231-158-0. La evidencia científica actual respalda que los dispositivos médicos fabricados a partir de aleaciones de acero que contienen cobalto no aumentan el riesgo de cáncer ni efectos adversos reproductivos. Para obtener más información, consulte el sitio web de la ECHA: Página de inicio - ECHA
Reacciones adversas
Las reacciones adversas y las posibles complicaciones asociadas a los dispositivos de fijación, como el sistema de fijación permanente CapSure™, pueden incluir, entre otras: hemorragia, dolor, edema y eritema en el sitio de la herida; septicemia o infección; recidiva de la hernia o dehiscencia de la herida, erosión y respuesta alérgica en pacientes con sensibilidad conocida al PEEK y a metales contenidos en acero inoxidable 316L, como cromo, níquel, cobre y hierro.